いま世界に拡がるウイルスは、
リアルタイムで追跡できるほど進化が速い。ウイルスはいわゆる生物ではないが、
私たちヒトを含む生物と共進化する存在だ。
世界的な分子系統学者である著者が、
躍動感みなぎる“進化の舞台”へ読者を誘う。

著者プロフィール
長谷川政美(はせがわ まさみ)
1944年生まれ。進化生物学者。統計数理研究所名誉教授。総合研究大学院大学名誉教授。理学博士(東京大学)。著書に『分子系統学』(岸野洋久氏との共著)『DNAに刻まれたヒトの歴史』(共に岩波書店)、『系統樹をさかのぼって見えてくる進化の歴史』(ベレ出版)、『世界でいちばん美しい進化の教室』(監修、三才ブックス)、『共生微生物からみた新しい進化学』(海鳴社)、『進化38億年の偶然と必然』(国書刊行会)など多数。1993年に日本科学読物賞、1999年に日本遺伝学会木原賞、2005年に日本進化学会賞・木村資生記念学術賞など受賞歴多数。全編監修を務める「系統樹マンダラ」シリーズ・ポスターの制作チームが2020年度日本進化学会・教育啓発賞を受賞。

ウイルスという存在
ーヒトの進化にどうかかわってきたのかー
第6話
ヒト・コロナウイルスの進化
文と写真 長谷川政美
◎SARSコロナウイルスの起源
SARSコロナウイルス「SARS-CoV」は、新型コロナウイルスであるSARSコロナウイルス2型「SARS-CoV-2」の親戚であり、2002年に中国広東省から世界中に広まった「SARS(重症急性呼吸器症候群)」を引き起こしたウイルスである。これに近縁なウイルスが最初広州の市場(図6-1)で食用動物として売られていたジャコウネコ科のハクビシン(図6-2)から採取されたために、最初SARSはもともとハクビシンがもっていたウイルスがヒトに感染するようになったものと考えられた。
ところが、第4話に登場した武漢ウイルス学研究所の石正麗(Zheng-Li Shi)らのグループは、キクガシラコウモリ(図6-3)を宿主とする多様なコロナウイルスの存在を明らかにした。その結果、SARSはキクガシラコウモリを自然宿主とするコロナウイルスの中から、ハクビシンを中間宿主とするものが現われ、それがヒトに感染するようになったと考えられた。



石正麗らのグループは、2011~2015年の5年間にわたって中国雲南省昆明近くのある一つの洞窟で野生コウモリからのコロナウイルスの採取を行なった。
2002年のSARSの流行は広東省から始まったが、広東省に棲息するコウモリからはSARS-CoVの起源にすぐに結びつくほど近縁なウイルスは得られなかったので、いろいろな所を調査して最終的にこの洞窟にたどり着いたのである。
雲南省のこの洞窟には、キクガシラコウモリ科のチュウゴクキクガシラコウモリ(Rhinolophus sinicus)、キクガシラコウモリ(Rhinolophus ferrumequinum; 図6-3)、ナカキクガシラコウモリ(Rhinolophus affinis)、それにカグラコウモリ科のストリクズカミツバカグラコウモリ(Aselliscus stoliczkanus)などさまざまな種類のコウモリが集まって生息している。石らは、これらのコウモリから15種類にもおよぶSARSr-CoVを採取することに成功した。そして、これらのウイルスのゲノム配列から思いがけないことが明らかになった(1)。
15種類のSARSr-CoVのゲノム間の塩基配列の相同性(共通祖先に由来する類似性)は、92.0~99.9%であるが、これらの配列とヒトやハクビシンのSARS-CoVとの間の相同性は、それまで知られていたコウモリのSARSr-CoVの相同性よりも高かったのである。従って、SARSの起源に迫る上で一歩前進したことになる。
雲南省の洞窟にいるコウモリから採取されたSARSr-CoVと、SARS-CoVとの間の最も顕著な違いは、スパイクたんぱく質遺伝子にあった。このたんぱく質はこれまでにも当連載にたびたび出てきたが、コロナウイルスが宿主細胞に感染する際に重要な働きをする。
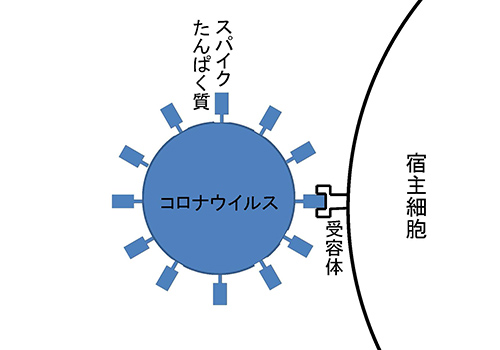
スパイクたんぱく質の受容体結合領域では、15種類のコウモリSARSr-CoVとSARS-CoVとの間の相同性がアミノ酸で78.2~97.2%と大きく変動する。しかも、コウモリ1個体に2種類のSARSr-CoVが感染していることもあり、組換えによって受容体結合領域の遺伝子がしばしば取り換えられているのである。
雲南省の洞窟で採取されたコウモリSARSr-CoVの中で、SARS-CoVと、スパイクたんぱく質の受容体結合領域の相同性が一番高いのはチュウゴクキクガシラコウモリを宿主とする「Rs4874」であった。しかし、この領域でコロナウイルスが感染して細胞に侵入する際に特に重要な働きをする6カ所のアミノ酸座位だけに注目すると、かなり違っていることが分かる(表6-1)。
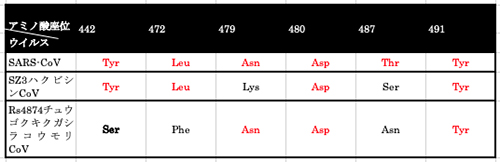
これらのアミノ酸座位は、SARS-CoV-2関連ウイルスについて第4話の表4-1で示した座位(455, 486, 493, 494, 501, 505)に対応するものである。
Rs4874はヒトのSARS-CoVとは6カ所のアミノ酸のうちの3つが違っている(表6-1の黒字)。またハクビシンのSZ3でも、6カ所のアミノ酸のうちの2つは違っている。ハクビシンに感染したウイルスの中で、さらに2つのアミノ酸変異を引き起こしたウイルスが、ヒトへの感染力を高めたものと考えられる。
さらに興味深いことに、15種類のSARSr-CoVの中でSARS-CoVに一番相同性が高いのは、比較する遺伝子によって違っている。このことは、この洞窟のコウモリの集団では多様なSARSr-CoVが感染しており、これらの間で組換えを繰り返していて、たまたまハクビシンやヒトに感染しやすい能力をもった遺伝子の組み合わせが実現して、パンデミックにつながったことを示唆する。
◎MERS-CoVの起源
「MERS(中東呼吸器症候群)」は、2012年にサウジアラビアから広まった「MERS-CoV」による感染症である。このウイルスは、もともとはアフリカに生息するケープクビワコウモリ(Neoromicia capensis)を自然宿主とするものが、家畜のヒトコブラクダ(図6-4)を中間宿主とするようになり、それがヒトに感染するようになったと考えられる(5)。
ウイルスが感染しても、自然宿主のコウモリは目立った症状を呈さないが、ヒトコブラクダは風邪のような症状を示すという。ところがヒトに感染すると、10%もの致死率の重篤な症状を引き起こす。

ケープクビワコウモリCoVとMERS-CoVのゲノム間の相同性は、アミノ酸レベルでは97%を超えるが、塩基レベルでは85%程度に過ぎない。コロナウイルスの突然変異率を1.04x10-3/塩基/年と仮定すると、15%の塩基の違いを生み出すのに必要な時間は、0.15/2/(1.04x10-3) = 72年になる。
ヒトコブラクダCoVはMERS-CoVとゲノムの配列はあまり違わない。ケープクビワコウモリCoVがMERS-CoVに一番近い親戚だとすると、およそ72年前にケープクビワコウモリからヒトコブラクダに感染したウイルスが、2012年になってヒトコブラクダからヒトに感染するようになったものと考えられる。これに先立つ20年前にアフリカでヒトコブラクダから採取された血清にこのウイルスが感染していた証拠が見られるという(5)。
新型コロナウイルスSARS-CoV-2の場合には、ヒトに感染したウイルスはすべて最初に武漢で採取されたウイルスの子孫であったが(図2-2)、MERS-CoVの場合はヒトコブラクダから繰り返しヒトに感染しているのだ(5)。
◎コロナウイルスの多様な起源
ヒトに感染するコロナウイルスとしては、21世紀に入ってからパンデミックを引き起こしたSARS-CoV 、SARS-CoV-2、MERS-CoV以外に、風邪のコロナウイルスが4種類知られている。図6-5にこれら7種類の「ヒト・コロナウイルス(Human coronavirus; HCoV)」とそれと近縁なウイルスをあわせた系統樹を示す。
ただし、これまでにも出てきたように、コロナウイルスの進化では組換えがしばしば起るので、必ずしもすべての遺伝子がこの系統樹に従うわけではない。
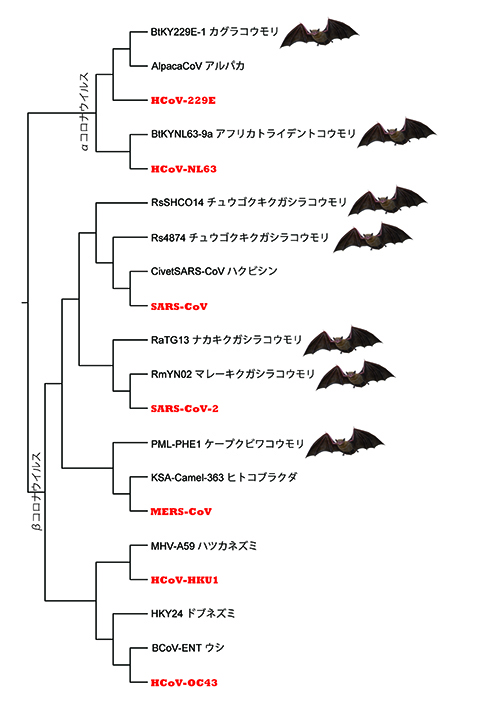
ここで注目すべきことは、7種類のHCoV(赤字)のうち、5種類がもともとコウモリを自然宿主としていたと考えられるものが、中間宿主(SARS-CoVはハクビシン、MERS-CoVはヒトコブラクダなど)を介してあるいは介さずに(中間宿主が知られていないだけかもしれないが)、ヒトに感染するようになったものだということである。残りの2種類の風邪のウイルス(「HKU1」と「OC43」)は、げっ歯類を自然宿主としていたものが、ヒトに感染するようになったものである。
SARS-CoV 、SARS-CoV-2、それにMERS-CoVは新興感染症コロナウイルスと呼ばれるが、そのほかのヒト・コロナウイルスが4種類の風邪ウイルスである。風邪の病原体は200種類以上あり、その90%はウイルスである。中でも一番多いのがライノウイルスだが、コロナウイルスが原因の風邪もあるのだ。
新興感染症コロナウイルスはすべてヒトに対して重篤な症状を引き起こすが、風邪のウイルスが引き起こす症状はそれらにくらべるとはるかに軽い。これら風邪のウイルスが最初にヒトに感染するようになった頃の状況は不明であるが、最初は新興感染症コロナウイルスのように重篤な病気を引き起こしていたのかもしれない。
これら風邪コロナウイルスの中で、一番最近になってヒトに感染するようになったと考えられるのが、「HCoV-OC43」である。普通の風邪のおよそ10%がこのウイルスによるものだという。
HCoV-OC43の自然宿主はドブネズミであるが、ゲノム配列からは中間宿主と考えられるウシのウイルスと分かれたのが、1890年頃だったと推定される(6)。
1889~1890年に流行したインフルエンザに似た感染症は、インフルエンザウイルスによるものだった考えられているが、もしかしてこれがHCoV-OC43のヒトへの最初の感染だったのかもしれない。同じ頃、感染力と致死率の高いウシの呼吸器系疾患もあったという。当時、ウイルスを解析する技術はなかったので、これらの感染症の実体は不明であるが、現在では軽い風邪のウイルスになっているHCoV-OC43が、最初にヒトに感染するようになった頃はもっと重篤なものであったことを示しているのかもしれない。
1.Hu, B. et al. (2017) Discovery of a rich gene pool of bat SARS-related coronaviruses provides new insights into the origin of SARS coronavirus. PLoS Pathog. 13(11), e1006698.
2.Forni, D. et al. (2017) Molecular evolution of human coronavirus genomes. Trends Microbiol. 25, 35-48.
3.Tao, Y. et al. (2017) Surveillance of bat coronaviruses in Kenya identifies relatives of human coronaviruses NL63 and 229E and their recombination history. J. Virol. 91, e01953-16.
4.Cui, J., Li, F., Shi, Z.-L. (2019) Origin and evolution of pathogenic coronaviruses. Nature Rev. Microbiol. 17, 181-192.
5.Corman, V.M. et al. (2014) Rooting the phylogenetic tree of Middle East respiratory syndrome coronavirus by characterization of a conspecific virus from an African bat. J. Virol. 88, 11297-11303.
6.Vijgen, L. et al. (2005) Complete genomic sequence of human coronavirus OC43: molecular clock analysis suggests a relatively recent zoonotic coronavirus transmission event. J. Virol. 79, 1595–1604.
*もっと「進化」について知りたい人の入門書:
☆本連載が本になりました!
長谷川政美著『ウイルスとは何か:生物か無生物か、進化から捉える本当の姿』 (中公新書)。ウイルスは恐ろしい病原体か、あらゆる生命の源か――。進化生物学の最前線から、その正体に迫る。

☆いちばん新しい本!
長谷川政美著『進化生物学者、身近な生きものの起源をたどる
』 (ベレ出版)。 イヌやネコやクマなど身近な生き物はすべて進化していまここにいる。もちろんヒトも。生き物の進化が一目でわかる「系統樹マンダラ」を多数掲載(系統樹の「見方」付き)。ささやかな「現代版 種の起原」ができました。

☆はじめの一冊にオススメ!
長谷川政美監修・畠山泰英構成『世界でいちばん素敵な進化の教室
』 (三才ブックス)。 本書は美しい写真とQ&A形式の簡潔な文章で、38億年におよぶヒトを含む生き物の進化を解説した超入門ビュアルブックです。子供から大人まで気軽に楽しんでいただけます。
4刷(2022年10月)。





