いま世界に拡がるウイルスは、
リアルタイムで追跡できるほど進化が速い。ウイルスはいわゆる生物ではないが、
私たちヒトを含む生物と共進化する存在だ。
世界的な分子系統学者である著者が、
躍動感みなぎる“進化の舞台”へ読者を誘う。

著者プロフィール
長谷川政美(はせがわ まさみ)
1944年生まれ。進化生物学者。統計数理研究所名誉教授。総合研究大学院大学名誉教授。理学博士(東京大学)。著書に『分子系統学』(岸野洋久氏との共著)『DNAに刻まれたヒトの歴史』(共に岩波書店)、『系統樹をさかのぼって見えてくる進化の歴史』(ベレ出版)、『世界でいちばん美しい進化の教室』(監修、三才ブックス)、『共生微生物からみた新しい進化学』(海鳴社)、『進化38億年の偶然と必然』(国書刊行会)など多数。1993年に日本科学読物賞、1999年に日本遺伝学会木原賞、2005年に日本進化学会賞・木村資生記念学術賞など受賞歴多数。全編監修を務める「系統樹マンダラ」シリーズ・ポスターの制作チームが2020年度日本進化学会・教育啓発賞を受賞。

ウイルスという存在
ーヒトの進化にどうかかわってきたのかー
第5話
SARS-CoV-2の今後
文と写真 長谷川政美
今回はCOVID-19がこれからどのように推移していくかについて考えてみよう。そこにはたくさんの複雑な要因が関わってくる。
◎ウイルス変異の可能性高めるパンデミック
前回(第4話)、SARS-CoV-2の進化速度が系統によってあまり変わらないことを見たが、これはあくまでもそれぞれの系統に沿ってウイルスのゲノムが変化していく速度が違わないという意味である。
感染が多くのひとに拡がれば、それだけ多くのウイルスの系統が生み出されるということだから、全体としては多様な変異が生まれることになる。長期的にはさまざまな変異の中から、ウイルス自身にとってより適応した変異が正の自然選択の結果として残っていくであろう。
平均的には、感染力を高めつつも、宿主であるヒトに対して致死的なダメージを与えないような変異が残っていくことが予想されるかもしれない。なぜなら、ウイルスが生き残って子孫を広めていくためには、理屈の上ではそのような変異が有利だと思われるからである。しかし、単純にそのように言い切ることはできない。
この文章を書いている時点(2020年10月28日)ではまだ、SARS-CoV-2は世界中で猛威を振るい続けている。このパンデミックが今後どのように推移していくかは、ウイルス自身が今後どのように進化していくかに依存するが、それにはこのウイルスに対してヒトの社会および免疫系がどのように対応するかということが関わってくる。ヒトの側の対応の仕方が、ウイルスの進化の仕方を決める選択圧になる。
SARS-CoV-2に感染すると免疫ができるが、それがどのくらいの期間持続し、次に感染した時にどの程度有効に働くかについては、不明なことが多い。また免疫のでき方はひとによって異なり、感染しても無症状のひとには、あまり免疫ができないという(1)。一度罹ったひとが再感染することもある。
麻疹(はしか)は一度罹ると一生免疫が持続するといわれているが(実際には免疫は減衰するが、流行が時々起こるので無症状で再感染をして免疫の抗体価を上げるということを繰り返していると考えられる)、SARS-CoV-2の免疫がそんなに長く持続することはないと思われる。次回の連載で、風邪のコロナウイルスの話をするが、この場合は感染して治ってから一年以内に再び同じウイルスに感染することはしばしば見られる。SARS-CoV-2に関してはまだデータが少ないが、2002年に流行したSARSに関しては免疫が2年間ほど持続するという報告がある(2)。しかし、SARSはすぐに終息したので、この免疫が再感染を防ぐ上でどの程度有効なのかということは確かめられていない。
先に述べたように、ウイルスは多くのひとに感染すればそれだけ多様な変異が生じることになる。そのような変異の中には、それ以前のウイルスに対して獲得された免疫が効かなくなるようなものもあるだろう。第2話で詳しく触れたように、SARS-CoV-2の表面にはスパイクたんぱく質などさまざまなたんぱく質があり、抗体は表面たんぱく質を認識してそれと結合する。従って、抗体が認識する表面たんぱく質の構造が変化すれば、抗体がそれを認識できなくなり免疫が効かなくなる。
◎半端な量・質の抗体では逆効果のことも
図5-1に抗体の構造の模式図を示した。ウイルスなどの抗原が体内に入ってくると抗体の抗原認識部位がウイルス表面の特徴を認識し、これと結合する。マクロファージなどの食細胞は抗体のFc受容体結合部位と結合できるFc受容体を持っており、この受容体を介して抗原と結合した抗体を認識して抗原を貪食する。こうして食細胞に飲み込まれた抗原は細胞内で破壊される。これが正常な免疫機構である。
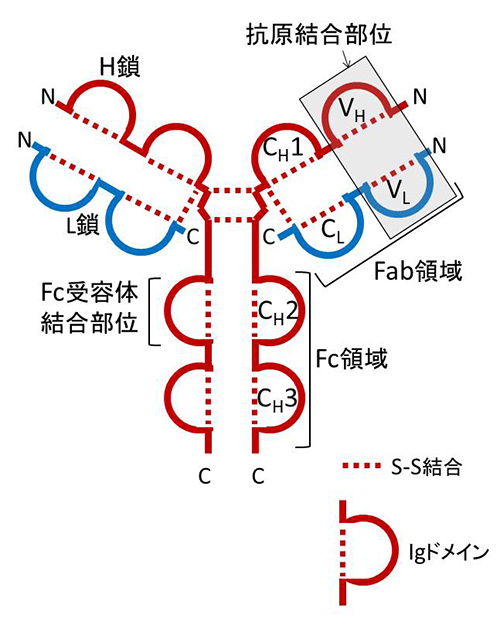
抗体つまり免疫グロブリン(Ig)は二本の長いポリペプチド(H鎖;heavy chain)と二本の短いポリペプチド(L鎖;light chain)から成る。それぞれのポリペプチドはいくつかのドメインから成る(H鎖は4個、Lは2個)。N末端(ポリペプチドのアミノ基で終わっている側の末端)付近の抗原結合部位は並列したH鎖のVHドメインとL鎖のVLドメインによって形成される。Vとは可変領域(variable region)という意味である。この領域は病原体などの抗原と結合する部位であり、膨大な数の異なる抗原を見分けることができるよう、多様なアミノ酸配列を生み出す仕組みがある。一人のヒトが作り得る可変領域の可能性は、多様なH鎖とL鎖の組み合わせで1000億以上にもなる。
このように多様な抗体を作り出す仕組みは、1980年代に利根川進らによって解明された。H鎖のC末端(カルボキシル末端)付近は定常領域(constant region)であり、Fc領域と呼ばれる。そこには、Fc受容体結合部位があり、マクロファージなどの白血球はこの部位と結合できる受容体(Fc受容体)を持っており、このFc受容体を介して抗原と結合した抗体を認識して抗原を貪食する。Fc領域が受容体と結合する反応は、可変領域に抗原が結合することによって引き起こされる。4本のポリペプチド同士やそれぞれのポリペプチド内にはいくつかのS-S結合(ジスルフィド結合)があり、それによって立体的な構造が保持される。
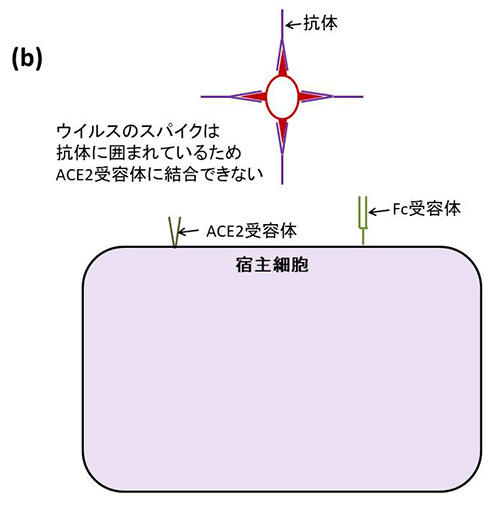
ウイルスに対する抗体が十分量あると、ウイルス粒子表面のスパイクたんぱく質は抗体に覆われてしまい、細胞に感染できなくなる(図5-2b)。
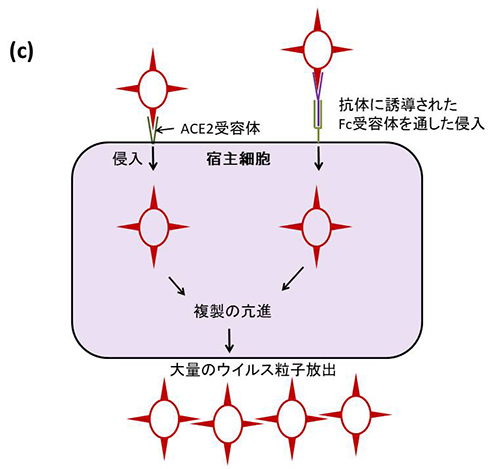
また抗体に覆われたウイルス粒子は、抗体と結合するFc受容体を表面にもつマクロファージなどに捕捉され、食作用で飲み込まれてしまい、細胞内で破壊される。ところが、抗体の量が十分でないと、図5-2cのように抗体と結合したウイルスがFc受容体を通して細胞内に侵入して増殖することがあるのだ。
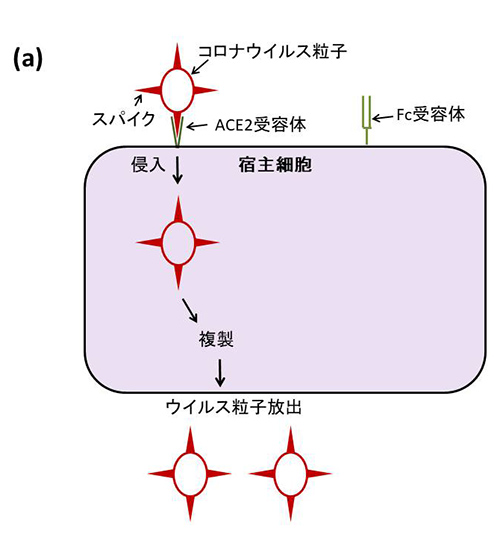
(a) SARS-CoV-2などのコロナウイルスに特異的な抗体がない場合は、ウイルスの膜に埋め込まれたスパイクたんぱく質は細胞表面のACE2(アンジオテンシン変換酵素2)受容体と結合し、細胞内に侵入する。コロナウイルスのまわりを包む膜は、細胞膜と同じ脂質二重膜であり、細胞と結合するとウイルスの膜が細胞膜と融合し、膜が裏返しになってウイルスは細胞の中に滑り込むのである。細胞内で複製を繰り返して増殖したウイルス粒子が細胞から放出され、ほかの細胞に感染が拡がる。ただし、すべてのコロナウイルスがACE2受容体を利用して感染するわけではない。ウイルスがどのような受容体を利用して感染するかによって、感染できる組織が決まる。
(b) 抗体が十分量あると抗体がウイルスのスパイクに結合し尽くすために、ウイルスは細胞のACE2受容体に結合できなくなり感染は起こらない。このように感染を防ぐために有効に働く抗体を中和抗体という。マクロファージなどの白血球は抗体の定常領域と結合するFc受容体を発現しており、それにより抗体で覆われたウイルスを貪食して細胞内で破壊する。
(c ) ところが、抗体量が十分でないと、抗体に結合したウイルスがFc受容体を通して細胞に侵入し、複製することがある。そのため抗体がウイルスの増殖を助けることになるので、これを「抗体依存性感染増強」(ADE)という。抗体の量がある閾値を下回ると、ADEが誘発される。有効な中和抗体として働くためには抗体濃度がある閾値以上ないとだめなのだ。
Fc受容体は主にマクロファージなど免疫系の食細胞がもつものであり、すべての細胞がもつわけではないが(ウイルス受容体も限られた細胞しかもたない)、食細胞に侵入したウイルスは破壊されることなく複製され、次の細胞に感染すべく、大量のウイルス粒子として放出される。これを「抗体依存性感染増強」(Antibody-dependent enhancement; ADE)という(4,5)。ウイルスが抗体を利用して感染し、複製するということである。抗体の量が少ないとなぜFc受容体をもつ細胞内でウイルスが破壊されないで複製の亢進(こうしん)が起こるのか、その機構の詳細は不明であるが、実際にこのような現象があるのだ。
ウイルスは宿主細胞に侵入するためにさまざまな細胞表面分子を利用するが、免疫が十分でないと、免疫系の仕組みさえも逆手にとって利用しているようなのである。抗体は通常感染症に対する防御機構と考えられるが、状況によっては抗体が逆にウイルスの増殖を助けることがあるのだ。正常な免疫系が働いている状態では、マクロファージに貪食されたウイルスは細胞内で破壊されるが、ウイルスがその仕組みを逃れて細胞内で大量に複製して放出されることがあるのだ。
ウイルス感染症の中には、一度感染したあとで以前の株から少し変異した別のウイルス株に感染すると、はじめて感染したひとよりも重症化することがあるという(6)。
デング熱はデングウイルスというプラス鎖一本鎖RNAウイルスによって引き起こされるが、このウイルスには4種類の型がある。そのうちの一つの型に感染して治ったひとは、その型のウイルスに対しては長期間の免疫を保持し続ける。ところが、別の型のウイルスに再感染すると、はじめてのひとよりもはるかに重篤になることがあるという(7)。このような現象は最初の感染で得られた抗体が十分な働きをしないために起きるADEによると考えられる。
コロナウイルスの中には、ネコに伝染性腹膜炎という致死的な病気を引き起こすものがある。1990年にオランダ・ユトレヒト大学のグループがこのウイルスのスパイクたんぱく質に対するワクチンを開発してネコに接種し、続いてこのウイルスに感染させる実験を行ったところ、対照群のネコよりもはるかに早く死亡したという(8)。これもADEによるものであろう。
抗体が認識する抗原部位(エピトープという)が少し変異していると、ADEが起こりうることがSARS-CoVを用いたアカゲザルでの実験で確かめられている(9)。ワクチンはウイルス表面のエピトープを認識する抗体を作ることによって免疫力を高めるよう設計されるが、ADEの潜在的な可能性はワクチン開発にあたって大きな問題となる(10)。ワクチンを接種したために、実際に感染した場合に接種しなかったひとよりも重篤になることもあるのだ(5)。
今後SARS-CoV-2の感染拡大が続けば、エピトープの変異が起こるであろう。一度罹って免疫が続いているひとでも、新しい型のエピトープをもったウイルスに感染するとADEが起こる可能性があるのだ。エピトープの変異がなくても、無症状や軽症で済んだひとでは抗体量が十分でないので、次に罹ったときにはADEが起こるかもしれない(11)。SARS-CoV-2に関しては、ADEが実際の問題になり得るかどうかについては否定的な意見もあるが(7)、ワクチン開発にあたってADEの潜在的な可能性を考慮することは必須であろう。
また現在開発中のSARS-CoV-2に対するワクチンの中のあるものは、エイズウイルスHIVの感染リスクを高めるという指摘がある(12)。従ってこのワクチンがSARS-CoV-2に対していかに有効であっても、現在でもエイズの流行が続いているサハラ以南のアフリカでは使えない。COVID-19の拡大を食い止めるためには有効なワクチンが必要であるが、ワクチン開発にはさまざまな問題があり、乗り越えなければならないたくさんの壁がある。
◎大気汚染とSARS-CoV-2
化石燃料による大気汚染が、SARS-CoV-2による重症化リスクに関連しているという研究がある(13)。PM2.5と呼ばれる直径が2.5マイクロメートル(0.0025ミリメートル)以下の超微小粒子による大気汚染は、呼吸器疾患などさまざまな病気の原因になると考えられている。新しい研究ではPM2.5による大気汚染が、SARS-CoV-2が細胞に感染する際に利用する細胞表面の受容体であるアンジオテンシン変換酵素2(ACE2)を活性化し、このウイルスに感染しやすくしている可能性があるという。
同じ受容体を使ってコロナウイルスが感染する2002年~2003年のSARS-CoVの流行でも、大気汚染がひどい地域の住民の致死率は空気がきれいな地域の住民にくらべて高かったという。第3話でCOVID-19の重症化リスクを高めるとされるネアンデルタール人由来の遺伝子をもつひとの割合が多いヨーロッパ諸国にくらべて、それが少ない東アジアの日本や韓国では感染したひとの中で死亡したひとの割合、つまり致死率が低いという話をした。そこでは触れなかったが、実は日本や韓国と同様の遺伝子組成の中国ではそれらの国にくらべて致死率が高いのである。日本と韓国における致死率がそれぞれ1.9%、1.7%なのに対して、武漢を含む湖北省では6.6%、中国全体の平均でも5.2%に達する。最初の流行地であり、医療崩壊がこのような高い致死率をもたらした面はあるが、近年の中国の大都市における大気汚染は深刻であり、それも一つの要因になっているのではないかと思われる。
皮肉なことに、COVID-19による都市封鎖や経済活動の縮小によって中国の大都市での大気汚染は大分改善されたが(14)、パンデミックが収まったあと再び元に戻ることがあってはならない。SARS-CoV-2が終息しても、再び似たような感染症が出現するであろう。大気汚染がわれわれの健康に及ぼす悪影響は、これまでに考えられていた以上に広範なものなのである。
◎SARS-CoV-2の今後
SARS-CoV-2が今後どのように進化していくかは、いろいろな要因が関わっていてはっきりと予測することはできない。感染拡大の様相、それに対する人間の側の対処法、とりわけワクチンや治療薬などが、ウイルスに対して選択圧として働き、ウイルス進化の方向を決めることになる。有効なワクチンが開発され、世界中で普及するようになればウイルスは行き場を失って絶滅する。天然痘ウイルスはそのようにして自然界からは絶滅した。また家畜のウシの重篤な感染症であり、その流行が世界史を変えたという牛疫を引き起こした牛疫ウイルスもワクチンにより絶滅させることに成功した。ところが、これまでそれ以外のウイルスでそのようにうまくいった例はない。
絶滅にまでいかなくても、宿主を死に至らしめるような重篤な症状を引き起こすウイルスは、弱毒化する方向に進化することが多い。しかし、抗体依存性感染増強の例などで見たように、ウイルスと宿主の間の関係には予測できないことが起こり得るのだ。
1. Long, Q.-X. et al. (2020) Clinical and immunological assessment of asymptomatic SARS-CoV-2 infections. Nature Med. 26, 1200-1204.
2. Mo, H. et al. (2006) Longitudinal profile of antibodies against SARS-coronavirus in SARS patients and their clinical significance. Respirology 11, 49-53.
3. アブル・アバス、アンドリュー・リクマン、シフ・ピレ(2018)『分子細胞免疫学』中尾篤人監訳、エルゼビア・ジャパン.
4. Kulkarni, R. (2020) Antibody-dependent enhancement of viral infections. In “Dynamics of Immune Activation in Viral Diseases”, Bramhachari, P.V. (ed.), pp. 9-41, Springer. https://doi.org/10.1007/978-981-15-1045-8_2.
5. Tirado, S.M.C., Yoon, K.-J. (2003) Antibody-dependent enhancement of virus infection and disease. Viral Immnol. 16, 69-86.
6. Eroshenko, N. et al. (2020) Implications of antibody-dependent enhancement of infection for SARS-CoV-2 countermeasures. Nature Biotech. 38, 788-797.
7. Peeples, L. (2020) Avoiding pitfalls in the pursuit of a COVID-19 vaccine. Proc. Natl. Acad. Sci. USA 117, 8218-8221.
8. Vennema, H. et al. (1990) Early death after feline infectious peritonitis virus challenge due to recombinant vaccinia virus immunization. J. Virol. 64, 1407-1409.
9. Wang, Q. et al. (2016) Immunodominant SARS coronavirus epitopes in humans elicited both enhancing and neutralizing effects on infection in non-human primates. ACS Infect. Dis. 2, 361-376.
10. Iwasaki, A., Yang, Y. (2020) The potential danger of suboptimal antibody responses in COVID-19. Nature Rev. Immunol. 20, 339-341.
11. Shaman, J., Galanti, M. (2020) Will SARS-CoV-2 become endemic? Science 10.1126/science.abe5960.
12. Buchbinder, S.P. et al. (2020) Use of adenovirus type-5 vectored vaccines: a cautionary tale. Lancet https://doi.org/10.1016/S0140-6736(20)32156-5.
13. Pozzer, A. et al. (2020) Regional and global contributions of air pollution to risk of death fromCOVID-19. Cardiovas. Res. doi:10.1093/cvr/cvaa288
14. Chen, K. et al. (2020) Air pollution reduction and mortality benefit during the COVID-19 outbreak in China. Lancet Planet Health 10.1016/S2542-5196(20) 30107-8.
*もっと「進化」について知りたい人の入門書:
☆本連載が本になりました!
長谷川政美著『ウイルスとは何か:生物か無生物か、進化から捉える本当の姿』 (中公新書)。ウイルスは恐ろしい病原体か、あらゆる生命の源か――。進化生物学の最前線から、その正体に迫る。

☆いちばん新しい本!
長谷川政美著『進化生物学者、身近な生きものの起源をたどる
』 (ベレ出版)。 イヌやネコやクマなど身近な生き物はすべて進化していまここにいる。もちろんヒトも。生き物の進化が一目でわかる「系統樹マンダラ」を多数掲載(系統樹の「見方」付き)。ささやかな「現代版 種の起原」ができました。

☆はじめの一冊にオススメ!
長谷川政美監修・畠山泰英構成『世界でいちばん素敵な進化の教室
』 (三才ブックス)。 本書は美しい写真とQ&A形式の簡潔な文章で、38億年におよぶヒトを含む生き物の進化を解説した超入門ビュアルブックです。子供から大人まで気軽に楽しんでいただけます。
4刷(2022年10月)。








